Личный кабинет информационной системы «Приоритет-2030»
Программа развития вуза«Приоритет-2030» на 2025-2036 гг.
Программа развития вуза «Приоритет-2030»
Отчет о результатах реализации программы развития университета в рамках«Приоритет-2030» за 2021 г.
Отчет о результатах реализации программы развития университета в рамках«Приоритет-2030» за 2022 г.
Новости
12 марта 2025 года ПСПбГМУ им. И.П. Павлова представил ежегодный отчет по программе «Приоритет-2030»
Представили итоги работы нашего университета по программе "Приоритет-2030" ректор ПСПбГМУ им. И.П. Павдова Сергей Фёдорович Багненко, проректор по послевузовскому образованию, профессор кафедры общественного здоровья и здравоохранения с курсом экономики и управления здравоохранением Константин Сергеевич Клюковкин, проректор по научной работе, заведующий кафедрой гематологии, трансфузиологии и трансплантологии с курсом детской онкологии ФПО имени профессора Б.В. Афанасьева, директор НИИ детской онкологии, гематологии и трансплантологии им. Р.М. Горбачевой Александр Дмитриевич Кулагин, начальник управления научных исследований Марина Олеговна Попова и заведующий кафедрой физики, математики и информатики, старший научный сотрудник научно-исследовательского центра биоинформатики НОИ биомедицины Артем Валерьевич Тишков. Подробнее

В рамках реализации программы стратегического академического лидерства «Приоритет-2030» в 2024 году был реализован проект создания конгресс-центра, располагающегося на базе Университета.
Конгресс-центр ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России - это многофункциональное пространство с комфортными залами для проведения различных мероприятий самого высокого уровня. Конференц-залы оборудованы всем необходимым для проведения мероприятий: столами президиума, трибунами, проекторами, экранами, плазменными панелями, звуковым оборудованием, имеется возможность проведения онлайн трансляций с видеоконференцсвязью. Центр располагает зонами питания для организации кофе-брейков, а также залом для индивидуального обслуживания гостей. Подробнее
Быть на вершине стоматологического прогресса! В ПСПбГМУ им. И.П. Павлова открылся стоматологический тренинг-центр Progressus.
5 декабря в рамках празднования 65-летия стоматологического факультета ПСПбГМУ им. акад. И. П. Павлова состоялось торжественное открытие стоматологического тренинг-центра Progressus. Проект реализован в рамках программы стратегического академического лидерства Минобрнауки России «Приоритет-2030» на функциональной основе кафедры стоматологии терапевтической и пародонтологии. Подробнее
Первый российский препарат генной клеточной терапии, допущен к проведению клинических исследований на людях после проведения доклиники на генетически модифицированных мышах, введенных в практику ПСПбГМУ им. И.П. Павлова в рамках реализации программы стратегического академического лидерства Минобрнауки России «Приоритет-2030».
11 ноября 2024 г. НМИЦ гематологии получил разрешение Минздрава России на проведение I-II фазы клинических исследований первого CAR-T-клеточного геннотерапевтического лекарственного препарата для терапии определенных видов рака крови — Утжефра (гемагенлеклейцел). Исследование, в которое будет включено около 60 пациентов, планируется завершить к концу 2025 г.
Ранее в 2023 г. НМИЦ завершил доклиническое исследование с использованием мышиной модели созданной ПСПбГМУ им. акад. И.П. Павлова совместно с НМИЦ им. В.А. Алмазова.
Это первый случай, когда одобрили исследование соматоклеточного генотерапевтического препарата на людях на основе исследований на животных, проведенных в РФ. Теперь доклинические исследования можно проводить целиком в России – что существенно облегчает и ускоряет исследовательский цикл.
Проконсультировать коллег об исследованиях на описываемой мышиной модели готов руководитель отдела биотехнологий Научно-исследовательского института детской онкологии, гематологии и трансплантологии им. Р.М. Горбачевой ПСПбГМУ им. И.П. Павлова Кирилл Викторович Лепик, тел.: +7 911 783 95 08.
В Первом Санкт-Петербургском государственном медицинском университете имени И.П. Павлова внедрено электронное расписание занятий. Работы проводятся в ходе выполнения планов цифровой трансформации в рамках реализации программы стратегического академического лидерства Минобрнауки России «Приоритет-2030»(национальный проект «Наука и университеты»).
Теперь обучающиеся имеют возможность просматривать расписание на своих мобильных устройствах и компьютерах, что гарантирует удобный доступ к необходимым данным в любое время в любом месте. В числе плюсов и то, что студенты могут получить доступ к расписанию через социальную сеть «ВКонтакте» без подключения специальных сервисов. Подробнее
30 сентября – 1 октября 2024 г. делегация ПСПбГМУ им. И.П. Павлова приняла участие во Всероссийском форуме "Медицинские университеты в Приоритете 2030", который проходил в Приволжском исследовательском медицинском университете Минздрава РФ в Нижнем Новгороде. Форум собрал более 40 медицинских университетов России, представителей научных организаций, федеральных экспертов и индустриальных партнеров вузов, создавая уникальную платформу для обмена опытом и поиска решений в области медицинского образования.
На фото делегация ПСПбГМУ им. И.П. Павлова:
Проректор по учебной работе Ярёменко Андрей Ильич,
Проректор по послевузовскуму образованию Клюковкин Константин Сергеевич,
Проректор по безопасности и развитию Стожаров Вадим Владимирович,
Начальник организационно-методического отдела управления научных исследований Хрусталев Максим Борисович,
Руководитель отдела биотехнологий Лепик Кирилл Викторович,
Аспирант Прокофьева Алина Аркадьевна
На дискуссионных площадках обсудили задачи по цифровой трансформации медицинского образования с целью подготовки специалистов нового поколения, выработали стратегические решения по достижению технологического лидерства в вопросах здоровьесбережения, оценили реалии и перспективы внедрения в структуру медуниверситетов научных проектных офисов как ключевых инструментов управления в вузе. Подробнее
16 июля 2024 года в аудитории №7 состоялось вручение дипломов по переподготовке на цифровой кафедре ПСПбГМУ им. И.П. Павлова. Дипломы получали обучающиеся, успешно освоившие программы "Основа веб программирования", "Язык Python в биомедицине", "Медицинская информатика" и "Биомедицинская статистика на языке R".
В этом году дипломы получили 477 выпускников цифровой кафедры, созданной в Университете в рамках программы стратегического академического лидерства Минобрнауки России «Приоритет-2030» (национальный проект «Наука и университеты»).
Доклад заведующей лабораторией генной и клеточной терапии отдела биотехнологий НИИ ДОГиТ им. Р.М. Горбачёвой ПСПбГМУ им. И.П. Павлова Алёны Игоревны Шакировой был признан лучшим на VII Конгрессе гематологов России, прошедшем 11-13 апреля в Москве. Поздравляем!
Отдельно отметим, что Министр здравоохранения России Михаил Альбертович Мурашко в своей приветственной речи к участникам конгресса отметил исследования ученых ПСПбГМУ им. И.П. Павлова по созданию первого российского CAR-T клеточного препарата, эффективно воздействующего на В-клеточные опухоли. Исследование реализуется в рамках программы Минобрнауки России «Приоритет 2030» (нацпроект «Наука и университеты»).

Ученые Первого Санкт-Петербургского государственного медицинского университета имени И.П. Павлова и Петербургского института ядерной физики имени Б.П. Константинова НИЦ «Курчатовский институт» запатентовали препарат для лечения болезни Паркинсона на ранних стадиях.
Он воздействует на фермент глюкоцереброзидазу, который кодируется геном GBA1. Мутации в нем в десять раз увеличивают риск развития патологии. Испытания на клетках пациентов показали, что созданная учеными молекула восстанавливает активность фермента.
«При снижении активности глюкоцереброзидазы в клетках накапливается субстрат. Он может стабилизировать нейротоксичные формы белка альфа-синуклеина, которые вызывают нейродегенерацию. Разработанная нами молекула собирает фермент таким образом, что он работает эффективнее», — рассказала руководитель отдела молекулярно-генетических и нанобиологических технологий Научно-исследовательского центра ПСПбГМУ им. И.П. Павлова Минздрава России, заведующая лабораторией молекулярной генетики человека НИЦ «Курчатовский институт» — ПИЯФ Софья Николаевна Пчелина. Подробнее
Известия - Быть в ферменте: в России запатентовали лекарство от болезни Паркинсона
Петербургский дневник - Ученые из Петербурга смогли запатентовать лекарство от болезни Паркинсона
Утро на Радио Звезда. Российские ученые запатентовали лекарство от болезни Паркинсона
26-28 февраля 2024 года в ПСПбГМУ им. И.П. Павлова Минздрава России прошла проектно-аналитическая сессия, организованная «Центром социологических исследований» («Социоцентр»), в рамках организационно-технического, информационного, методического, экспертно-аналитического сопровождения программы стратегического академического лидерства Минобрнауки России «Приоритет-2030» (национальный проект «Наука и университеты»).
Сессия состоялась в нашем Университете уже в третий раз. В ней приняли участие трое экспертов ФГАНУ «Социоцентр» и университетские специалисты разных уровней и профилей.
В рамках сессии эксперты, сотрудники и обучающиеся университета обсудили ключевые вопросы стратегии развития и трансформации университета, существующей системы проектного управления в университете, эффективность базовых и текущих процессов внутри университета, проанализировали возможности по выстраиванию эффективной внутренней и внешней коммуникации. В ходе работы эксперты делились ценным опытом и дали ряд рекомендаций.
13 февраля в рамках сессии «Генная терапия: вчера, сегодня, завтра» с докладом выступила руководитель направления генной клеточной терапии Научно-исследовательского института детской онкологии, гематологии и трансплантологии имени Р.М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета имени академика ПСПбГМУ им. И.П. Павлова Министерства здравоохранения Российской Федерации к.м.н. Марина Олеговна Попова. Подробнее
Комиссия Минобрнауки России подвела ежегодные итоги реализации вузами базовой части гранта государственной программы поддержки университетов «Приоритет-2030» и расширила финансирование ПСПбГМУ им. И.П. Павлова в рамках программы. Подробнее
ПСПбГМУ им. И.П. Павлова представил ежегодный отчет по программе «Приоритет 2030»
В этом гуду представили итоги работы нашего университета по программе "Приоритет2030" ректор ПСПбГМУ им. И.П. Павдова Сергей Фёдорович Багненко, в рамках совместной работы в консорциуме Директор-главный конструктор Государственного научного центра Российской Федерации "Центральный научно-исследовательский и опытно-конструкторский институт робототехники и технической кибернетики"(ГНЦ РФ ЦНИИ РТК) Александр Витальевич Лопота, заведующий кафедрой гематологии, трансфузиологии, трансплантологии факультета послевузовского образования имени профессора Б.В. Афанасьева, директор НИИ детской онкологии, гематологии и трансплантологии им. Р.М. Горбачевой Александр Дмитриевич Кулагин, декан факультета фундаментальной медицины ПСПбГМУ им. И.П. Павлова Иван Сергеевич Моисеев и доцент кафедры гематологии, трансфузиологии и трансплантологии с курсом детской онкологии ФПО им. проф. Б.В. Афанасьева Марина Олеговна Попова. Подробнее

Ученые ПСПбГМУ им. И.П. Павлова разрабатывают новый оригинальный российский продукт генной клеточной терапии для лечения онкологических и аутоиммунных заболеваний, не поддающихся стандартному лечению
В стенах Первого Санкт-Петербургского государственного медицинского университета им. И.П. Павлова, в клинике научно-исследовательского института детской онкологии, гематологии и трансплантологии им. Р.М. Горбачевой, для лечения злокачественных опухолей пациентам каждый день выполняются протоколы химиотерапии и трансплантации костного мозга. Однако не все опухоли поддаются лечению этими методами. И здесь на помощь медикам приходит генная инженерия и синтетическая биология. Подробнее
Делегация ПСПбГМУ им. И.П.Павлова приняла участие в Priority Fest 2023: Фестивале лучших практик программы «Приоритет 2030».
12–13 октября в МГИМО состоялся PRIORITY FEST 2023 — фестиваль лучших практик вузов-участников и кандидатов программы «Приоритет 2030». Соорганизатором в этом году выступил оператор программы «Приоритет 2030» ФГАНУ «Социоцентр».
Мероприятие прошло во второй раз и вновь стало площадкой обмена накопленным опытом, инструментарием и экспертизой и по аналогии с прошлым годом соберет вместе ректоров и проректоров российских вузов, руководителей проектных офисов, стратегических и институциональных проектов университетов-участников «Приоритета 2030». Подробнее

Коллектив ученых Первого Санкт-Петербургского государственного медицинского университета имени академика И.П. Павлова (ПСПбГМУ имени академика И.П. Павлова) разработал оригинальную панель с расширенным списком генов для диагностики наследственных дислипидемий на платформе массового параллельного секвенирования. Разработка может помочь оперативно поставить верный диагноз и спасти жизнь пациенту с редким наследственным заболеванием. Подробнее

Так, с помощью диагностической панели у девочки дошкольного возраста с подозрением на семейную гиперхолестеринемию выявили две редкие мутации в гене ABCG8, что указало на наличие ситостеролемии. Это заболевание, при котором в крови и тканях накапливаются растительные жиры, в том числе ситостерол. В МГНЦ им. акад. Н.П. Бочкова на биохимическом обследовании у ребенка обнаружили превышение концентрации ситостерола в сыворотке крови. Это вещество растительного происхождения, по своей структуре похожее на холестерин. Таким образом, диагноз ситостеролемии был дополнительно подтвержден.
Исследование проводится в рамках программы Минобрнауки России «Приоритет 2030» (национальный проект «Наука и университеты»).
29 июня в ПСПбГМУ им. И.П. Павлова состоялось торжественное открытие лаборатории генной и клеточной терапии, созданной в рамках программы «Приоритет 2030».
Перерезали красную ленточку, торжественно открыв новую лабораторию, ректор ПСПбГМУ им. акад. И.П. Павлова Сергей Фёдорович Багненко и директор НИИ ДОГиТ им. Р.М.Горбачевой Александр Дмитриевич Кулагин. На открытии присутствовали проректор по научной работе, заведующий кафедрой анестезиологии и реаниматологии, руководитель научно-клинического центра анестезиологии и реаниматологии, профессор, академик РАН Юрий Сергеевич Полушин, директор научно-исследовательского центра, профессор кафедры патологической анатомии с патологоанатомическим отделением профессор Владимир Викторович Томсон, директор НИИ нефрологии, профессор кафедры пропедевтики внутренних болезней и кафедры нефрологии и диализа ФПО профессор Владимир Александрович Добронравов, а также другие сотрудники университет и студенты. Подробнее

Благодаря участию ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России в программе Приоритет 2030 22-25 июня 2023 произошло уникальное событие на территории нашего университета в 50 км от Санкт-Петербурга, на полуострове Зеленый мыс Лемболовского озера на учебно-спортивной базе «Васкелово». В рамках реализации программы развития Университета, коллективом НИИ ДОГиТ им. Р.М. Горбачевой совместно с коллегами из ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России проведен первый Ретрит по генной и клеточной терапии. Васкелово 2023. Подробнее

Ученые нашли способ повысить эффективность фототермической терапии при лечении злокачественных новообразований. Они предложили одновременное применение наночастиц селена и золота, а также создали специальные капсулы для их доставки к опухолевым клеткам.
Над научным проектом работали ученые из Института биомедицинских систем и биотехнологий подведомственного Минобрнауки России Санкт-Петербургского политехнического университета Петра Великого (СПбПУ), Первый Санкт-Петербургский государственный медицинский университет имени академика И. П. Павлова (лаборатория генной и клеточной терапии) (ПСПбГМУ), Санкт-Петербургский государственный химико-фармацевтический университет, (Виварий) (СПХФУ), Национальный Исследовательский Университет ИТМО, (Новый физтех).
Проект реализуется в рамках программы Минобрнауки России «Приоритет-2030», которая является одной из мер государственной поддержки университетов нацпроекта «Наука и университеты».
17 июня 2023 года ПСПбГМУ им. И.П. Павлова посетил помощник Заместителя Председателя Правительства Российской Федерации Д.Н. Чернышенко А.Н. Швиндт
На встрече также присутствовали начальник отдела управления информационно-аналитического сопровождения стратегических проектов ФГБУ «Российский центр научной информации» Шерегов А.Х., начальник отдела управления обеспечения работы с данными сферы исследований и разработок ФГБУ «Российский центр научной информации» Сергеев А.А. и группа сотрудников Университета, участвующих в реализации программы стратегического академического лидерства «Приоритет2030». Подробнее
29-31 мая 2023 года в ПСПбГМУ им. акад. И.П. Павлова прошла проектно-аналитическая сессия с экспертной группой «Центра социологических исследований» («Социоцентр»), который осуществляет организационно-техническое, информационное, методическое, экспертно-аналитическое сопровождение Программы «Приоритет - 2030»
В рамках сессии эксперты, сотрудники и обучающиеся университета обсудили ключевые вопросы стратегии развития и трансформации университета, существующей системы проектного управления в университете, проанализировали возможности по выстраиванию эффективной внутренней и внешней коммуникации. Подробнее
В рамках Программы «Приоритет 2030» в ПСПбГМУ им. И.П. Павлова была создана «Цифровая кафедра» и открыты две новые программы подготовки обучающихся — «Язык Python в биомедицине» и «Основы веб-программирования»
При современной динамике развития цифровых технологий довольно сложно предположить, какие навыки и умения в области программного обеспечения останутся узким специалистам, а какие станут «таблицами умножения» для каждого выпускника. В ПСПбГМУ им И.П. Павлова считают своевременным и современным обучать студентов-медиков азам программирования. Студенты активно записывались на два предложенных курса. Один из них посвящен развитию и разработке веб-сайтов и адаптирован под архитектуру медицинских информационных систем. Второй курс посвящен обработке биомедицинских данных и вопросам биомедицинской статистики и биоинформатики. В планах Цифровой кафедры ПСПбГМУ им. И.П. Павлова ежегодно пополнять запас программ на одну-две, а также представить реализуемые программы в виде онлайн-курсов. Подробнее
В марте 2023 года ПСПбГМУ им. И.П. Павлова зарегистрировал «Малое инновационное предприятие «Медико-академические решения и технологии» (ООО «МИП «МАРТ»)
В рамках программы «Приоритет 2030» МИП будет разрабатывать и поддерживать программное обеспечения и IT-решения для сопровождения научной деятельности учреждений, подведомственных Минздраву России и адаптацией существующего программного обеспечения к цифровым платформам организаций. Подробнее
ПСПбГМУ им. акад. И.П. Павлова на первом месте по количеству трансплантаций костного мозга
Европейское общество трансплантации костного мозга (EBMT) опубликовало в журнале Bone Marrow Transplantation (Passweg J. R. et al., 2023) свежий обзор, в котором описывается деятельность 694 трансплантационных центров из 44 стран Европы и 9 сотрудничающих неевропейских государств.
Согласно полученным данным, в 2021 году всего было выполнено 47 412 трансплантации гемопоэтических стволовых клеток (42 % аллогенных и 58 % аутологичных), при этом Российская Федерация находится на восьмом месте по количеству проведенных трансплантаций. ПСПбГМУ им. акад. И.П. Павлова (НИИ детской онкологии, гематологии и трансплантологии им. Р.М. Горбачевой, CIC 725) занимает первое место среди всех центров, выполнив 446 трансплантации (аллогенные – 64%). На втором месте по числу проведенных трансплантаций находится лондонская клиника University College Hospital, CIC 224, которая провела 346 процедур. Подробнее
Заседание комиссии Минобрнауки России по рассмотрению ежегодных отчётов университетов-участников программы «Приоритет 2030»
Началось подведение первых итогов работы университетов в рамках программы «Приоритет 2030». С 24 по 27 ноября команды вузов-получателей базовой части гранта представят отчеты о реализации программ развития за 2021-2022 годы. Решение о статусе вуза и его дальнейшем участии в «Приоритет 2030» примет комиссия Минобрнауки России.
Механизм ротации университетов, заложенный в «Приоритет 2030», предполагает возможность перемещения участников между треками. Вузы, получающие базовую часть гранта в размере 100 млн рублей, могут перейти в статус получателей специальной части гранта (до 1 млрд рублей). Университеты, не подтвердившие достижение заявленных ранее показателей, уступят место кандидатам на участие в программе.
24 ноября команда нашего Университета во главе с проректором по учебной работе Андреем Ильичом Ярёменко представила отчет об итогах работы в рамках программы "Приоритет 2030". Подробнее
Борьба с неврологическими заболеваниями продолжается.
Сегодня не существует окончательно подтвержденного способа лечения, который помог бы предотвратить или существенно замедлить такие неврологические заболевания, как Альцгеймер, Паркинсон, рассеянный склероз и другие. Ведущие учёные медицинских научных центров нашей страны продолжают искать решение. Благодаря исследованию, проведенному в консорциуме, в России появится возможность разработать лекарство, замедляющее изменения структур нервной системы.
- В ПСПбГМУ им. ак. И.П. Павлова выделили группу пациентов с наследственной формой заболевания, при которой гибель нейронов развивается из-за мутации в гене.
- В НИЦ «Курчатовский институт» — ПИЯФ удалось создать компьютерную модель дефектного белка и подобрать ряд химических соединений, способных восстанавливать его функцию.
- В Институте цитологии и генетики СО РАН г. Новосибирска оценили эффективность предложенных химических соединений на пациент-специфичных нейронах, полученных из клеток крови человека.
Разработка наших ученых может стать революционной в лечении основных неврологических расстройств.
Телеканал МИР. "Евразия. Дословно" - Сергей Багненко: Через 50 лет людей будет лечить врач с роботом-помощником
В этом году легендарному Первому Санкт-Петербургскому государственному медицинскому университету им. И. П. Павлова исполняется 125 лет. 10 из них ректором вуза работает академик РАН, главный внештатный специалист по скорой медицинской помощи Минздрава России, хирург Сергей Багненко. Как врачи справляются с выгоранием? Что необходимо поменять в системе платной медицины? Как изменился портрет абитуриента за последние десятилетия и не оставят ли современные технологии и искусственный интеллект врачей без работы? Смотрите эксклюзивное интервью в программе «Евразия. Дословно». Подробнее
Санкт-Петербургский вестник высшей школы. Ректорская практика - Человека, который решил стать врачом, ничто не остановит
Интервью с ректором Первого Санкт-Петербургского государственного медицинского университета им. акад. И. П. Павлова доктором медицинских наук, профессором, академиком РАН Сергеем Фёдоровичем Багненко.
— Расскажите, пожалуйста, о программе «Приоритет 2030» (были определены четыре стратегических проекта развития научной работы университета). В рамках этой программы университет получил значительную сумму на научные разработки.
— Сначала в рамках программы «Приоритет 2030» действительно было четыре проекта, но после года работы мы их объединили в один. Мы значительно продвинулись в генетических технологиях и избрали геномную медицину в качестве стратегического проекта, объединяющего лидирующие научно-¬клинические направления. Так, клиника университета является лидером в области трансплантации костного мозга и клеточной терапии. Еще в начале ¬1990-х годов, когда в результате устранения последствий Чернобыльской аварии был дан старт программе трансплантации, сотрудники университета выполнили — первыми в нашей стране — аллогенные трансплантации костного мозга. Тогда мир был открыт полностью, и наши сотрудники, в частности Борис Владимирович Афанасьев, который стажировался в США и Германии, привез эту технологию. Она у нас появилась раньше, чем у других в стране. Был сформирован институт — ныне Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачёвой, который специализируется на процедуре трансплантации. Сейчас с помощью этой технологии мы лечим онкологические заболевания, рассеянный склероз, орфанные и аутоиммунные заболевания. В настоящий момент во всем мире научная область трансплантации костного мозга трансформируется благодаря появлению новых молекулярных технологий, открывающих перспективы генной клеточной терапии. Для работы в этом направлении у нас сформирован мощный коллектив. Ежегодно мы проводим международный форум по новым технологиям и понимаем, что можем оказаться, с точки зрения генной терапии, в лидерах. Для этого нам нужна специальная научно-производственная лаборатория, государство уже помогает в ее организации. Потенциал данных технологий очень высок. Например, у человека можно взять его лимфоциты, в них произвести искусственную модификацию определенного рецептора и получить невосприимчивость этого человека к ВИЧ-инфекции. А если это сделать с уже заболевшим ВИЧ, то потенциально возможно достичь выздоровления и прекратить прием антиретровирусной терапии. Конечно, требуются дополнительные исследования, инфраструктура и новые специалисты, для того чтобы внедрить эти технологии в практическую деятельность. И в этом заключается важнейшая роль вуза как участника программы «Приоритет 2030». Вместе с проведением научных исследований мы планируем готовить в этом направлении специалистов и даже целые команды, которые будут применять технологию в других регионах России. Наш университет все свои проекты формирует вокруг этого и движется дальше по программе «Приоритет 2030». Подробнее
Совместными усилиями исследователей трех столиц было выявлено соединение, которое может стать первым отечественным лекарственным препаратом, способным предотвращать нейродегенерацию. Проведенные в рамках программы «Приоритет 2030» исследования являются прекрасной предпосылкой для создания консорциума ведущих научно-исследовательских центров страны, а именно: ПСПбГМУ им. ак. И.П. Павлова, НИЦ «Курчатовский институт» - ПИЯФ, ИЦиГ СО РАН и ФГБНУ «МГНЦ», а разработанная технология может быть использована для создания препаратов направленного действия при других патологиях человека. Подробнее
Первый канал. Премии за заслуги в образовании вручил премьер-министр Михаил Мишустин
Россия 1. Вести в 20:00. Эфир от 04.10.2022. Лучшие педагоги страны получили премии от правительства
Премии Правительства Российской Федерации в области образования получили сотрудники подведомственных организаций Минобрнауки России
Ученые из Санкт-Петербурга нашли эффективный способ контроля за развитием заболевания COVID-19
Российские ученые установили причины опасного снижения показателей липидного спектра крови при COVID-19
Недавно исследования, проведенные в мире, продемонстрировали, что для тяжелого течения COVID-19 характерно значительное снижение основных показателей липидного спектра плазмы крови, а именно уровня общего холестерина и переносящих его частиц липопротеинов, происходящее на фоне цитокинового шторма. Низкий уровень холестерина липопротеинов низкой плотности в разных исследованиях ассоциировался с неблагоприятным прогнозом заболевания.
Команде врачей и исследователей из ПСПбГМУ им. ак. И.П. Павлова удалось не только подтвердить эти находки в ходе проспективного наблюдения пациентов, поступавших в отделение интенсивной терапии, но также установить возможные причины этого явления. Важную роль в открытии сыграли передовые геномные технологии: был проведен анализ транскриптома иммунных клеток пациентов с различным клиническим исходом. Данный анализ позволяет сделать выводы об активности генов. Подробнее

Приоритет 2030: вызовы нового времени
Новые технологии генной инженерии быстро развиваются и врываются в медицину, изменяя ее кардинально. Само понятие мишени в разработке новых методов лечения меняется – теперь мы можем управлять болезнью на уровне генетического кода, аккуратно изменяя его для преодоления болезни. Новая область медицины – генная и клеточная терапия – изменение последовательности генома соматических клеток для коррекции заболевания становится реальностью и ставит новые задачи для медицинской науки, практики и образования врачей нового поколения. Детальное изучение генетики опухоли и пациента позволяет подобрать наиболее эффективную персонализированную траекторию лечения.
Сформулировано основное направление стратегического проекта – Университетский Центр Геномной Медицины и основное направление развития. Университет должен стать лидирующим центром науки и подготовки кадров в Российской Федерации в области здравоохранения и геномных технологий, осуществляющий интеграцию научной, образовательной и практической деятельности для удовлетворения потребностей личности, общества и государства. Все проводимые в первый год мероприятия были направлены на реализацию этой цели и становление университета в качестве лидирующего научного, образовательного и клинического центра геномных технологий.
Для удовлетворения новых потребностей Университет трансформируется. В 2022 году в Университете открыта новая лаборатория, цель которой расширить научно-исследовательскую активность в области генной инженерии и расширить линейку продуктов для разработки в Университете и проведения доклинических исследований существующих продуктов генной и клеточной терапии, над которыми сотрудники университета работают последние несколько лет. Создан пайплайн диагностических и терапевтических генетических продуктов. Линейка таких продуктов включает разработку новых технологий лечения / продуктов генной и клеточной терапии для лечения ВИЧ инфекции у пациентов со злокачественными заболеваниями кроветворной и лимфатической ткани (лимфомы и лейкозы), для лечения резистентных В-клеточных опухолей, гемоглобинопатий и наследственных синдромов с нарушением клеточного состава крови и иммунного ответа. Помимо работы над продуктами, новая лаборатория решает фундаментальные научные задачи, редактирования генома гемопоэтических стволовых клеток, работает над проблемой невирусной доставки инструментов редактирования генома и встраивания в геном «гена интереса», и результаты этих исследований были представлены в качестве постерного доклада на самой знаменитой площадке в области генной и клеточной терапии, ежегодной конференции американского общества клеточной и генной терапии в 2022 году. Диагностическое звено реализуется на площадках ранее существовавших клинических лабораторий молекулярной биологии, и включает широкий спектр методик для применения в онкологии, кардиологии, гематологии, трансплантации органов и тканей.
16 сентября 2021 в рамках XV международного симпозиума «Трансплантация гемопоэтических стволовых клеток. Генная и клеточная терапия» в ПСПбГМУ им. И.П. Павлова прошел день генной и клеточной терапии, который стал крупнейшей в России площадкой по обсуждению клинического применения методов генной терапии в Российской Федерации. Несмотря на ограничения, связанные с пандемией COVID-19, в дне генной терапии приняли участие более 30 очных участников и более 200 он-лайн участников. Выступали ведущие специалисты в области генной терапии: Ханс-Питер Ким (Сиэтл), Борис Фезе (Гамбург), Федор Урнов (Беркли), Мария Эстер Бернардо (Милан), Джулина Феррари (Милан), Джерард Вагемакер (Роттердам), Сергей Куцев (Москва), Михаил Масчан (Москва), Клаудио Муссолино (Фрайбург), Денис Сабатино (Филадельфия), Мишель Саделаин (Нью-Йорк). Также на площадке были представлены успехи ведущих отечественных центров в области генной терапии: данные по CAR-T разработкам представили НМИЦ им. В.А. Алмазова, НМИЦ им. Д. Рогачева, ИКМБ СО РАН. Все материалы конференции доступны для просмотра (https://rgmm.info/translyacii/konferenc-zal-master).

Симпозиум освящал последние достижения в области разработки генетических конструктов для клинического применения, методов эпигенетической регуляции, методы контроля безопасности и off-target эффекта. Также площадка симпозиума стала местом для дискуссии в области регуляторных аспектов разработки и применения продуктов генной терапии. В обсуждении проблем и путей решения принимали участие представители фармацевтической индустрии, венчурных фондов, представители академических разработчиков, регуляторных органов и благотворительных организаций. Работа площадки, безусловно, послужила сближению позиций и приближению внедрения продуктов генной терапии в Российской Федерации.
В образовательную программу Университета внесен раздел обучения врачей-гематологов клиническому ведению пациентов, получающих CAR-T терапию. Внесены изменения в постдипломные программы переподготовки:
- Профессиональная переподготовка по специальности «Гематология»: «Гематология» — 504 часа
- «Актуальные вопросы гематологии и трансплантации костного мозга» — 144 часов
- «Терапия Т-клетками с химерным антигенным рецептором (CAR-T)» — 18 часов
В 2021-2022 году профессиональную переподготовку в включением образовательных материалов по CAR-T прошли 49 врачей.
Слушатели программы ПП «Гематология» 504 академических часа:
осень 2021 — 7 гематологов.
весна 2022 — 3 гематолога
Программа ПК «Актуальные вопросы гематологии и ТКМ» 144 академических часа:
осень 2021 — 10
весна 2022 — 12
Модуль НМО «Терапия Т-клетками с химерным антигенным рецептором» 18 академических часа:
осень 2021 — 12
весна 2022 — 5
Новая медицина требует специалистов нового поколения, и Университет открывает новый факультет фундаментальной медицины, где будут учить врачей-исследователей с новыми навыками для удовлетворения потребностей в специалистах в области генной и клеточной терапии как для академических учреждений, так и для индустрии по специальностям врач-биохимик и врач-биофизик. Набор планируется открыть уже в 2023 году.
Одним из важных направлений программы Университетского центра геномной медицины является CAR-T терапия. CAR-T представляют собой лимфоциты пациента, с помощью генетической модификации вооружённые для уничтожения опухоли. Этот тип терапии требует высокотехнологичного и безопасного процесса производства генно-модифицированных Т-клеток. Одним из этапов в разработке собственного процесса производства CAR-T ПСПбГМУ им. ак. И.П. Павлова является создания вирусного вектора, доставляющего генетический материал – химерный антигенный рецептор - в Т-лимфоциты пациента, перенаправляя их активность для уничтожения опухоли.
С 23 июня по 16 июля сотрудники Университета в рамках консорциума были направлены в Институт молекулярной и клеточной биологии Сибирского отделения РАН для реализации важного компонента программы доклинических исследований CAR-T: масштабирование производства лентивирусных векторов до клинических объемов. Была выполнена работа по разработке оптимальных условий производства вирусного вектора для CAR-T терапии. Был произведён скрининг основных параметров по наработке вектора в культуре клеток и его очистке. Полученные результаты приближают внедрение метода CAR-T терапии в клиническую практику Университета.

За период реализации программы Приоритет 2030 в клиническую практику внедрены следующие диагностические генетические методики:
|
Оценка длины теломер и экспрессии генов белков шелтериного комплекса : Теломеры – это концевые участки хромосом, которые определяют вероятность потери генетического материала при делении клеток. Длина теломер является суррогатным маркером «старения» и пролиферативного потенциала соматических клеток. Методика определения длины теломер известна достаточно давно, тем не менее, разработана не только отечественная методика, которая существенно дешевле коммерческих иностранных лабораторных наборов, но метод усовершенствован определением экспрессии белков шелтериного комплекса, которые защищают теломеры и определение их количества дополняет клиническую прогностическую значимость анализа. Определение длинны теломер используется для определения качества трансплантата гемопоэтических стволовых клеток и качества клеточных продуктов. Разработка является неотъемлемой частью создания полного цикла разработки генно-модифицированных продуктов. |
 |
|
| Диагностическая панель обогащения для секвенирования нового поколения в отношении генов DICER1 и DROSHA. Гены DICER1 и DROSHA отвечают за кодирование ферментов процессинга микроРНК и отвечают за синтез большинства этих регуляторных молекул. Мутации в этих генах встречаются при широком спектре злокачественных заболеваний и влияют на патогенез и прогноз, тем не менее данные гены не входят в большинство таргетных панелей секвенирования. На основании исследования генетики пациентов с опухолями крови и биоинформатического анализа удалось составить оригинальную панель для таргетного секвенирования. В настоящий момент проходит ее клиническая валидация. |  |
|
|
Панели экспрессионных маркеров лейкемических стволовых клеток: В настоящий момент в онкологии и гематологии все чаще не рентгенологический/гематологический ответ опухоли является целью терапии, а достижение статуса отрицательной минимальной остаточной болезни, т.е. состояния, когда невозможно определить наличие опухолевых клеток методами молекулярной биологии или проточной цитометрии. К сожалению, до половины опухолей в зависимости от заболевания не обладают характерными генетическими характеристиками, которые бы позволяли отслеживать остаточные опухолевые клетки. Альтернативной методикой является выявление «подписи» генов характерных для лейкемических стволовых клеток. У взрослых и детей они различаются. У взрослых важен профиль активности генов WT1, BAALC и EVI1. Для детей важны гены DNMT3b, GPR56, СD34, SOCS2, SPINK2 и FAM30A. Профиль этих генов позволяет предсказывать рецидив миелоидных лейкозов и персонализировать терапию. |
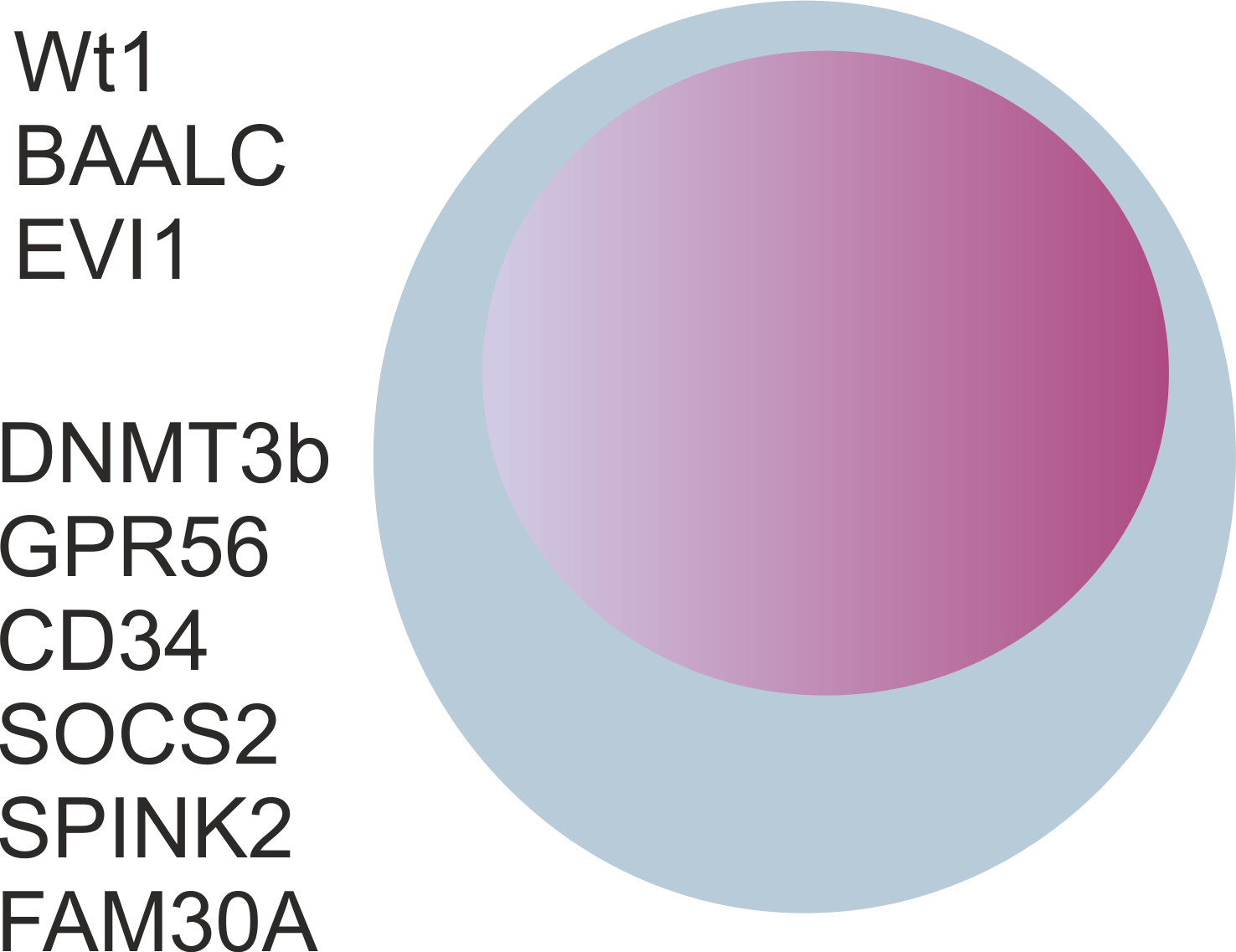 |
|
|
Тест потери HLA: Одним из механизмов рецидива после HLA-частично совместимой аллогенной трансплантации гемопоэтических стволовых клеток является потеря антигенов главной гистосовместимости. Частота такой клональной эволюции составляет до 30% всех рецидивов лейкозов у детей и взрослых. До этого в РФ отсутствовал доступ к этому анализу. Тест крайне важен для принятия решения о повторной трансплантации гемопоэтических столовых клеток или таргетной терапии. За время реализации Приоритета 2030 эта методика разработана и проходит клиническую валидацию. |
 |
|
|
16S секвенирования для оценки состояния микробиоты при лечении онкологических заболеваний: В последние годы методы секвенирования микробиоты позволили понять значительную роль микробиоты в патогенезе и модуляции иммунного ответа при злокачественных опухолях. Современное онкологическое лечение на сегодняшний день сложно себе представить без детализированной картины состава микробиоты кишечника. Эта информация позволяет как эффективно лечить инфекционные осложнения более прецизионной антибактериальной терапией, так и накапливать знания в отношении роли микробиоты в течении основного онкологического заболевания. Хотя в настоящий момент существуют только грубые методы коррекции, такие как трансплантация фекальной микробиоты, тем не менее, накапливаемые знания станут основой для создания инновационных анаэробных бактериальных препаратов. Хотя в настоящий момент многие учреждения реализуют 16S секвенирование, представляется невозможным существование Университетского Центра Геномной Медицины без этого анализа. |
 |
|
| Экзомное секвенирование и анализ мутационного профиля у пациентов с костномозговой недостаточностью: Костно-мозговая недостаточность представлена двумя большими группами болезней: врожденные (генетические) и приобретенные (иммунные). Провести различия между ними зачастую возможно только проведя детальные анализ более 500 генов, кроме этого постоянно выявляются новые мутации в ранее не описанных генах. В клиническую практику Университета был внедрено секвенирование и биоинформатический анализ «клинического» экзома для диагностики этой группы заболеваний. При этом, результаты анализа являются критическими, так как определяют возможность и эффективность аллогенной трансплантации гемопоэтических стволовых клеток. Составленная база пациентов не кандидатов на трансплантацию может стать основой для разработок персонализированной генной терапии. |  |
Университет в соответствии с детализированным пайплайном терапевтических продуктов за первый год сфокусировал свои усилия на нескольких основных направлениях:
|
Отечественный продукт анти-CD19 CAR-T: Это генетически модифицированные иммунные клетки пациента с онкологическим заболеванием "вооруженные" при помощи генетической модификации искусственно созданным рецептором, специфичным к маркеру на поверхности опухолевых клеток. CAR-T произвели революцию в лечении В клеточных лимфом и острого лимфобластного лейкоза, и в настоящий момент технология тестируется в отношении других, более распространенных видов опухолей. Процесс производства этого "живого лекарства" индивидуализирован, поскольку CAR-T изготавливаются из собственных (аутологичных) иммунных клеток, и может быть затруднен, если в результате болезни или интенсивного предшествующего лечения, число и функция собственных иммунных клеток недостаточна. Технология "аллогенных" CAR-T, т.е. произведенных из клеток здоровых доноров может приблизить применение этого метода к алгоритмам использования обычных лекарств, и сделать его более доступным. Однако создание аллогенных CAR-T является сложной задачей с биологической точки зрения, требующей внесения нескольких генетических изменений, в том числе с применением технологии редактирования генома. За время первого года участия в программе Приоритет разработана детализированная дорожная карта доклинических и клинических исследований, которая должна в конце 2023-2024 обеспечить доступ пациентов к этому варианту инновационного лечения. За 2022 проведены тестовые запуски производства CAR-T в закрытых системах: В настоящий момент разрабатывается альтернативный, не зависящий от импорта протокол производства. Проводятся работы по масштабированию производства лентивируса в количествах, достаточных для клинического применения, продолжаются доклинические исследования in vitro, сделаны первые эксперименты in vivo. |
 |
|
|
Ранние доклинические исследования «универсального» CAR-T: Среди методов иммунотерапии онкологических заболеваний в настоящий момент выделяются технологии применения биспецифических антител и клеток с химерным антигенным рецептором (CAR-T). Биспецифические антитела - это биологически молекулы создающие механический и биологический контакт между иммунными и опухолевыми клетками, что приводит к активации иммунных клеток и уничтожению опухоли. CAR-T это генетически модифицированные иммунные клетки пациента с онкологическим заболеванием "вооруженные" при помощи генетической модификации искусственно созданным рецептором, специфичным к маркеру на поверхности опухолевых клеток, и уничтожающие опухоль после распознавания мишени. Несмотря на то, что, обе технологии показали свою эффективность в лечении резистентных В клеточных опухолей, каждая из них имеет присущие ей ограничения. Коллективом молодых исследователей НИИ ДОГиТ им. Р.М. Горбачевой ПСПбГМУ им. ак. И.П.Павлова, совместно с коллегами из ИМКБ СО РАН был предложен оригинальный дизайн молекулярной структуры химерного антигенного рецептора, который позволяет совместить технологию CAR-T и биспецифических антител. Предложенный принцип заключается в "перенаправлении" специфичности CAR-T с помощью разных видов биспецифических антител, что может позволить регулировать активность генетически модифицированных клеток, или задать несколько вариантов их специфичности. Коллективом был произведен синтез генетических фрагментов, кодирующих рецептор, и эксперименты in vitro, свидетельствующие об активации полученных CAR-T при добавлении антител в присутствии клеток-мишеней (клеточной линии В-клеточной лимфомы). Продолжаются доклинические исследования. |
 |
|
|
CCR5 Knock-out гемопоэтические столовые клетки и лимфоциты: В течение длительного времени Университет делал фокус на отработку технологии аутологичной и аллогенной трансплантации гемопоэтических стволовых клеток у пациентов с опухолями крови и ВИЧ-инфекцией, как основу для последующей реализации генной терапии. Работа по модификации стволовых клеток находится на поздних доклинических стадиях и этой проект является наиболее продвинутым на настоящий момент продуктом генной и клеточной терапии на настоящий момент. Результаты исследований будут оглашены в отдельном пресс-релизе. |
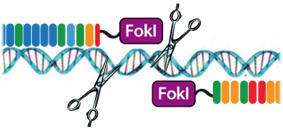 |
|
|
Невирусные средства доставки инструментов редактирования генома: Ключевой проблемой генной терапии является отсутствие эффективных и безопасных методов внутриклеточной доставки генетического материала. Тенденцией последних лет является замена вирусной трансфекции на невирусные методы доставки, такие как электропорация и использование синтетических микроносителей. Внедрение новых невирусных систем доставки генов позволит удешевить процедуры генной терапии, увеличить безопасность и таким образом, ускорить трансляцию методов генной терапии в клиническую практику. Научная тема посвящена разработке и внедрению новых методов генной терапии на основе модификации клеток гемопоэтического ряда, включая геномное редактирование, с целью излечения рефрактерных/рецидивирующих форм гематологических и онкологических заболеваний, а также наследственных заболеваний. За время участия в программе Приоритет 2030 оформлена концепция собственной платформы Университета для доставки генетического материала в ядро на основе полиэлектролитных капсул с карбонатным ядром и инкорпорацией в частицы ингибиторов РНК-каз. Разрабатываемая платформа позволяет добиться существенно больших процентов трансфекции, чем, например при электропорации или вирусной трансфекции, выполнить последующую селекцию трансфецированных клеток. Развитие этой платформы обеспечивают как большой потенциал для научных исследований, так и технологическую независимость Университетского Центра Геномной Медицины. |
 |
Подводя итог работы в программе «Приоритет 2030» можно с уверенностью сказать, что Университет объединяет на своей площадке классическую триаду, наука, клиника и образование и во всех областях трансформируется для удовлетворения потребностей нового времени, новой медицины.
1: Talianov PM, Peltek OO, Masharin M, Khubezhov S, Baranov MA, Drabavičius A,
Timin AS, Zelenkov LE, Pushkarev AP, Makarov SV, Zyuzin MV. Halide Perovskite
Nanocrystals with Enhanced Water Stability for Upconversion Imaging in a Living
Cell. J Phys Chem Lett. 2021 Sep 23;12(37):8991-8998. doi:
10.1021/acs.jpclett.1c01968. Epub 2021 Sep 13. PMID: 34514804.
2: Petit AF, Kulasekararaj AG, Eikema DJ, Maschan A, Adjaoud D, Kulagin A,
Grassi A, Fagioli F, Griskevicius L, Snowden JA, Johansson JJ, Dalle JH, Byrne
J, Risitano AM, Peffault de Latour R, Dufour C. Upfront unrelated donor
hematopoietic stem cell transplantation in patients with idiopathic aplastic
anemia: A retrospective study of the Severe Aplastic Anemia Working Party of
European Bone Marrow Transplantation. Am J Hematol. 2022 Jan 1;97(1):E1-E3. doi:
10.1002/ajh.26354. Epub 2021 Nov 28. PMID: 34553406.
3: Bug DS, Tishkov AV, Moiseev IS, Porozov YB, Petukhova NV. Towards
Understanding the Pathogenicity of DROSHA Mutations in Oncohematology. Cells.
2021 Sep 8;10(9):2357. doi: 10.3390/cells10092357. PMID: 34572006; PMCID:
PMC8471307.
4: Pagano L, Salmanton-García J, Marchesi F, Busca A, Corradini P, Hoenigl M,
Klimko N, Koehler P, Pagliuca A, Passamonti F, Verga L, Víšek B, Ilhan O, Nadali
G, Weinbergerová B, Córdoba-Mascuñano R, Marchetti M, Collins GP, Farina F,
Cattaneo C, Cabirta A, Gomes-Silva M, Itri F, van Doesum J, Ledoux MP, Čerňan M,
Jakšić O, Duarte RF, Magliano G, Omrani AS, Fracchiolla NS, Kulasekararaj A,
Valković T, Poulsen CB, Machado M, Glenthøj A, Stoma I, Ráčil Z, Piukovics K,
Navrátil M, Emarah Z, Sili U, Maertens J, Blennow O, Bergantim R, García-Vidal
C, Prezioso L, Guidetti A, Del Principe MI, Popova M, de Jonge N, Ormazabal-
Vélez I, Fernández N, Falces-Romero I, Cuccaro A, Meers S, Buquicchio C, Antić
D, Al-Khabori M, García-Sanz R, Biernat MM, Tisi MC, Sal E, Rahimli L, Čolović
N, Schönlein M, Calbacho M, Tascini C, Miranda-Castillo C, Khanna N, Méndez GA,
Petzer V, Novák J, Besson C, Duléry R, Lamure S, Nucci M, Zambrotta G, Žák P,
Seval GC, Bonuomo V, Mayer J, López-García A, Sacchi MV, Booth S, Ciceri F,
Oberti M, Salvini M, Izuzquiza M, Nunes-Rodrigues R, Ammatuna E, Obr A,
Herbrecht R, Núñez-Martín-Buitrago L, Mancini V, Shwaylia H, Sciumè M, Essame J,
Nygaard M, Batinić J, Gonzaga Y, Regalado-Artamendi I, Karlsson LK, Shapetska M,
Hanakova M, El-Ashwah S, Borbényi Z, Çolak GM, Nordlander A, Dragonetti G,
Maraglino AME, Rinaldi A, De Ramón-Sánchez C, Cornely OA; EPICOVIDEHA working
group. COVID-19 infection in adult patients with hematological malignancies: a
European Hematology Association Survey (EPICOVIDEHA). J Hematol Oncol. 2021 Oct
14;14(1):168. doi: 10.1186/s13045-021-01177-0. PMID: 34649563; PMCID:
PMC8515781.
5: Schmid C, Labopin M, Schaap N, Veelken H, Brecht A, Stadler M, Finke J,
Baron F, Collin M, Bug G, Ljungman P, Blaise D, Tischer J, Bloor A, Kulagin A,
Giebel S, Gorin NC, Esteve J, Ciceri F, Savani B, Nagler A, Mohty M. Long-term
results and GvHD after prophylactic and preemptive donor lymphocyte infusion
after allogeneic stem cell transplantation for acute leukemia. Bone Marrow
Transplant. 2022 Feb;57(2):215-223. doi: 10.1038/s41409-021-01515-3. Epub 2021
Nov 8. PMID: 34750562; PMCID: PMC8821014.
6: Fedorova LV, Lepik KV, Volkov NP, Kotselyabina PV, Borzenkova ES, Popova MO,
Beynarovich AV, Baykov VV, Kozlov AV, Moiseev IS, Mikhailova NB, Kulagin AD.
Efficacy and safety of nivolumab combined with brentuximab vedotin after
nivolumab monotherapy failure in patients with relapsed and refractory classic
Hodgkin lymphoma. Int J Clin Oncol. 2022 Mar;27(3):626-632. doi:
10.1007/s10147-021-02085-6. Epub 2021 Nov 26. PMID: 34826011; PMCID: PMC8619646.
7: Gusak A, Fedorova L, Lepik K, Volkov N, Popova M, Moiseev I, Mikhailova N,
Baykov V, Kulagin A. Immunosuppressive Microenvironment and Efficacy of PD-1
Inhibitors in Relapsed/Refractory Classic Hodgkin Lymphoma: Checkpoint Molecules
Landscape and Macrophage Populations. Cancers (Basel). 2021 Nov 12;13(22):5676.
doi: 10.3390/cancers13225676. PMID: 34830831; PMCID: PMC8616219.
8: Nagler A, Labopin M, Dholaria B, Wu D, Choi G, Aljurf M, Ciceri F, Gedde-
Dahl T, Meijer E, Niittyvuopio R, Bondarenko S, Bourhis JH, Cornelissen JJ,
Socié G, Koc Y, Canaani J, Savani B, Bug G, Spyridonidis A, Giebel S, Brissot E,
Bazarbachi A, Esteve J, Mohty M. Graft-versus-Host Disease Prophylaxis with
Post-Transplantation Cyclophosphamide versus Cyclosporine A and Methotrexate in
Matched Sibling Donor Transplantation. Transplant Cell Ther. 2022
Feb;28(2):86.e1-86.e8. doi: 10.1016/j.jtct.2021.11.013. Epub 2021 Nov 29. PMID:
34856420.
9: Bakin EA, Stanevich OV, Chmelevsky MP, Belash VA, Belash AA, Savateeva GA,
Bokinova VA, Arsentieva NA, Sayenko LF, Korobenkov EA, Lioznov DA, Totolian AA,
Polushin YS, Kulikov AN. A Novel Approach for COVID-19 Patient Condition
Tracking: From Instant Prediction to Regular Monitoring. Front Med (Lausanne).
2021 Dec 7;8:744652. doi: 10.3389/fmed.2021.744652. PMID: 34950678; PMCID:
PMC8688846.
10: Smirnov S, Petukhov A, Levchuk K, Kulemzin S, Staliarova A, Lepik K,
Shuvalov O, Zaritskey A, Daks A, Fedorova O. Strategies to Circumvent the Side-
Effects of Immunotherapy Using Allogeneic CAR-T Cells and Boost Its Efficacy:
Results of Recent Clinical Trials. Front Immunol. 2021 Dec 15;12:780145. doi:
10.3389/fimmu.2021.780145. PMID: 34975869; PMCID: PMC8714645.
11: Battipaglia G, Galimard JE, Labopin M, Raiola AM, Blaise D, Ruggeri A, Koc
Y, Gülbas Z, Vitek A, Sica S, Diez-Martin JL, Castagna L, Bruno B, Rovira M,
Moiseev I, Martino M, Grillo G, Araujo MC, Bulabois CE, Nguyen S, Socié G, Arat
M, Pavlu J, Tischer J, Martin H, Corral LL, Choi G, Forcade E, McDonald A, Pane
F, Bazarbachi A, Ciceri F, Nagler A, Mohty M. Post-transplant cyclophosphamide
in one-antigen mismatched unrelated donor transplantation versus haploidentical
transplantation in acute myeloid leukemia: a study from the Acute Leukemia
Working Party of the EBMT. Bone Marrow Transplant. 2022 Apr;57(4):562-571. doi:
10.1038/s41409-022-01577-x. Epub 2022 Jan 25. PMID: 35079140.
12: Albert MH, Slatter MA, Gennery AR, Güngör T, Bakunina K, Markovitch B,
Hazelaar S, Sirait T, Courteille V, Aiuti A, Aleinikova OV, Balashov D, Bernardo
ME, Bodova I, Bruno B, Cavazzana M, Chiesa R, Fischer A, Hauck F, Ifversen M,
Kałwak K, Klein C, Kulagin A, Kupesiz A, Kuskonmaz B, Lindemans CA, Locatelli F,
Lum SH, Maschan A, Meisel R, Moshous D, Porta F, Sauer MG, Sedlacek P, Schulz A,
Suarez F, Vallée TC, Winiarski JH, Zecca M, Neven B, Veys P, Lankester AC.
Hematopoietic stem cell transplantation for Wiskott-Aldrich syndrome: an EBMT
Inborn Errors Working Party analysis. Blood. 2022 Mar 31;139(13):2066-2079. doi:
10.1182/blood.2021014687. PMID: 35100336.
13: Gevorgian AG, Kozlov AV, Tolkunova PS, Kazantzev IV, Yukhta TV, Morozova EV,
Kulagin AD, Punanov YA, Zheludkova OG, Zubarovskaya LS. Tandem autologous
hematopoietic stem cell transplantation for embryonal brain tumors in infants
and very young children. Bone Marrow Transplant. 2022 Apr;57(4):607-612. doi:
10.1038/s41409-022-01593-x. Epub 2022 Feb 3. PMID: 35115669.
14: Baranova IB, Popova MO, Yaremenko AI, Zubkova NV, Pinegina ON, Nikolaev IY.
Invazivnyi mukormikoz s porazheniem organov chelyustno-litsevoi oblasti u
onkogematologicheskikh bol'nykh na fone khimioterapevticheskogo lecheniya i
transplantatsii gemopoeticheskikh stvolovykh kletok [Invasive mucormycosis
affecting maxillofacial region in oncohematological patients undergoing
chemotherapeutic treatment and transplantation of hematopoietic stem cells].
Stomatologiia (Mosk). 2022;101(2):80-86. Russian. doi:
10.17116/stomat202210102180. PMID: 35362708.
15: Rodríguez-Arbolí E, Labopin M, Eder M, Brecht A, Blau IW, Huynh A, Forcade
E, Tischer J, Bethge W, Bondarenko S, Verbeek M, Bulabois CE, Einsele H, Stölzel
F, Savani B, Spyridonidis A, Bazarbachi A, Giebel S, Brissot E, Schmid C, Nagler
A, Mohty M. Augmented FLAMSA-Bu versus FluBu2 reduced-intensity conditioning in
patients with active relapsed/refractory acute myeloid leukemia: an EBMT
analysis. Bone Marrow Transplant. 2022 Jun;57(6):934-941. doi:
10.1038/s41409-022-01611-y. Epub 2022 Apr 7. PMID: 35393528.
16: Bazarbachi A, Boumendil A, Finel H, Khvedelidze I, Romejko-Jarosinska J,
Tanase A, Akhtar S, Ben Othman T, Ma'koseh M, Afanasyev B, Cheikh J, Briones J,
Gülbas Z, Hamladji RM, Elverdi T, Blaise D, Martínez C, Alma E, Halaburda K,
Sousa AB, Glass B, Robinson S, Montoto S, Sureda A. The outcome of patients with
Hodgkin lymphoma and early relapse after autologous stem cell transplant has
improved in recent years. Leukemia. 2022 Jun;36(6):1646-1653. doi:
10.1038/s41375-022-01563-8. Epub 2022 Apr 12. Erratum in: Leukemia. 2022
Aug;36(8):2150. PMID: 35414657.
17: McLornan DP, Gras L, Martin I, Sirait T, Schroeder T, Blau IW, Kuball J,
Byrne J, Collin M, Stadler M, Desmier D, Salmenniemi U, Jindra P, Mikhailova N,
Lenhoff S, Rifón J, Robin M, Rovira M, Veelken H, Sadowska-Klasa A, Zecca M,
Hayden PJ, Czerw T, Hernández-Boluda JC, Yakoub-Agha I. Outcome of allogeneic
haematopoietic cell transplantation in eosinophilic disorders: A retrospective
study by the chronic malignancies working party of the EBMT. Br J Haematol. 2022
Jul;198(1):209-213. doi: 10.1111/bjh.18219. Epub 2022 Apr 28. PMID: 35482558.
18: Kulasekararaj AG, Griffin M, Langemeijer S, Usuki K, Kulagin A, Ogawa M, Yu
J, Mujeebuddin A, Nishimura JI, Lee JW, Peffault de Latour R; 301/302 Study
Group. Long-term safety and efficacy of ravulizumab in patients with paroxysmal
nocturnal hemoglobinuria: 2-year results from two pivotal phase 3 studies. Eur J
Haematol. 2022 Sep;109(3):205-214. doi: 10.1111/ejh.13783. Epub 2022 Jun 16.
PMID: 35502600.
19: Beynarovich A, Lepik K, Mikhailova N, Borzenkova E, Volkov N, Moiseev I,
Zalyalov Y, Kondakova E, Kozlov A, Stelmakh L, Pirogova O, Zubarovskaya L,
Kulagin A, Afanasyev B. Favorable outcomes of allogeneic hematopoietic stem cell
transplantation with fludarabine-bendamustine conditioning and
posttransplantation cyclophosphamide in classical Hodgkin lymphoma. Int J
Hematol. 2022 May 5. doi: 10.1007/s12185-022-03355-3. Epub ahead of print. PMID:
35511399.
20: Marchesi F, Salmanton-García J, Emarah Z, Piukovics K, Nucci M, López-
García A, Ráčil Z, Farina F, Popova M, Zompi S, Audisio E, Ledoux MP, Verga L,
Weinbergerová B, Szotkovski T, Da Silva MG, Fracchiolla N, De Jonge N, Collins
G, Marchetti M, Magliano G, García-Vidal C, Biernat MM, Van Doesum J, Machado M,
Demirkan F, Al-Khabori M, Žák P, Víšek B, Stoma I, Méndez GA, Maertens J, Khanna
N, Espigado I, Dragonetti G, Fianchi L, Del Principe MI, Cabirta A, Ormazabal-
Vélez I, Jaksic O, Buquicchio C, Bonuomo V, Batinić J, Omrani AS, Lamure S,
Finizio O, Fernández N, Falces-Romero I, Blennow O, Bergantim R, Ali N, Win S,
Van Praet J, Tisi MC, Shirinova A, Schönlein M, Prattes J, Piedimonte M, Petzer
V, Navrátil M, Kulasekararaj A, Jindra P, Sramek J, Glenthøj A, Fazzi R, De
Ramón-Sánchez C, Cattaneo C, Calbacho M, Bahr NC, El-Ashwah S, Cordoba R,
Hanakova M, Zambrotta G, Sciumè M, Booth S, Rodrigues RN, Sacchi MV, García-
Poutón N, Martín-González JA, Khostelidi S, Gräfe S, Rahimli L, Ammatuna E,
Busca A, Corradini P, Hoenigl M, Klimko N, Koehler P, Pagliuca A, Passamonti F,
Cornely OA, Pagano L. COVID-19 in adult acute myeloid leukemia patients: a long-
term followup study from the European Hematology Association survey
(EPICOVIDEHA). Haematologica. 2022 May 12. doi: 10.3324/haematol.2022.280847.
Epub ahead of print. PMID: 35545919.
21: Waszczuk-Gajda A, Penack O, Sbianchi G, Koster L, Blaise D, Reményi P,
Russell N, Ljungman P, Trneny M, Mayer J, Iacobelli S, Kobbe G, Scheid C,
Apperley J, Touzeau C, Lenhoff S, Jantunen E, Anagnostopoulos A, Paris L, Browne
P, Thieblemont C, Schaap N, Sierra J, Yakoub-Agha I, Garderet L, Styczynski J,
Schoemans H, Moiseev I, Duarte RF, Peric Z, Montoto S, van Biezen A, Mikulska M,
Aljurf M, Ruutu T, Kröger N, Morris C, Koenecke C, Schoenland S, Basak GW.
Complications of Autologous Stem Cell Transplantation in Multiple Myeloma:
Results from the CALM Study. J Clin Med. 2022 Jun 20;11(12):3541. doi:
10.3390/jcm11123541. PMID: 35743620; PMCID: PMC9225651.
22: Dedukh D, Riumin S, Kolenda K, Chmielewska M, Rozenblut-Kościsty B,
Kaźmierczak M, Ogielska M, Krasikova A. Maintenance of pure hybridogenetic water
frog populations: Genotypic variability in progeny of diploid and triploid
parents. PLoS One. 2022 Jul 6;17(7):e0268574. doi: 10.1371/journal.pone.0268574.
PMID: 35793279; PMCID: PMC9258834.
23: Bazarbachi A, Boumendil A, Finel H, Khvedelidze I, Romejko-Jarosinska J,
Tanase A, Akhtar S, Ben Othman T, Ma'koseh M, Afanasyev B, El-Cheikh J, Briones
J, Gülbas Z, Hamladji RM, Elverdi T, Blaise D, Martínez C, Alma E, Halaburda K,
Sousa AB, Glass B, Robinson S, Montoto S, Sureda A. Correction: The outcome of
patients with Hodgkin lymphoma and early relapse after autologous stem cell
transplant has improved in recent years. Leukemia. 2022 Aug;36(8):2150. doi:
10.1038/s41375-022-01639-5. Erratum for: Leukemia. 2022 Jun;36(6):1646-1653.
PMID: 35840758.
В Санкт-Петербурге разработали ультразвуковую технологию остановки кровотечений